Probablemente sea la primera vez que hayas escuchado juntos los términos “proteómica” y “úlcera”. Quizás también te haya llamado la atención que trate un tema de investigación básica en este blog, cuyo contenido suele estar estrechamente relacionado con la práctica clínica. Sin embargo, dado que los cambios proteómicos son claves para entender y tratar la úlcera venosa, no podía dejar de dedicar a este tema una entrada en el blog.
¿Y por qué he tenido la idea de hablar sobre proteómica? El “culpable” ha sido el Dr. Rodrigo Rial, cirujano vascular al que admiro y con el que siempre es un placer coincidir. “Proteómica de la úlcera venosa: modificación epigenética con terapia compresiva” fue el título de su excelente ponencia en el también excepcional IV congreso de la Sociedad Gallega de Heridas, que se acaba de celebrar en Vigo. “Estrategia terapéutica antiinflamatoria ante heridas en miembros inferiores” se titulaba la mía, y la terapia compresiva fue una gran protagonista. Dos formas de hablar de lo mismo: “úlcera venosa= inflamación crónica”. Aunque en otros post ya hemos tocado el tema del microambiente proinflamatorio en las heridas que no cierran, espero que esta entrada sobre “proteómica de la úlcera venosa” pueda inspirar a alguno de vosotros para seguir trabajando en esta línea de investigación, como hace el equipo del Dr. Rodrigo Rial.


¿Qué es la proteómica?
La proteómica es la rama de la biología que estudia el conjunto de proteínas expresadas por un genoma, una célula o un tejido (proteoma).
Hay muchos motivos que justifican el interés de estudiar las proteínas y no quedarnos sólo en los genes. En primer lugar, un gen puede dar lugar a diferentes proteínas y hay factores ambientales que pueden modificar la expresión genética (epigenética). Además, las proteínas van a sufrir diferentes modificaciones tras su producción para realizar su función. Y no podemos olvidar que las proteínas interaccionan entre ellas formando complejos proteicos, de los que dependerá su acción en las células. ¡Qué complejo e interesante es el proteoma?!
Para entender y tratar adecuadamente los daños en los tejidos humanos por diferentes patologías, es fundamental conocer las modificaciones en la cantidad y tipo de proteínas que se han producido o se están produciendo en esos tejidos. En otras palabras, tener una “fotografía del proteoma” nos da pistas sobre la actividad celular “anómala o destructiva” en las diferentes enfermedades.
¿Qué sabemos de proteómica en úlceras venosas?
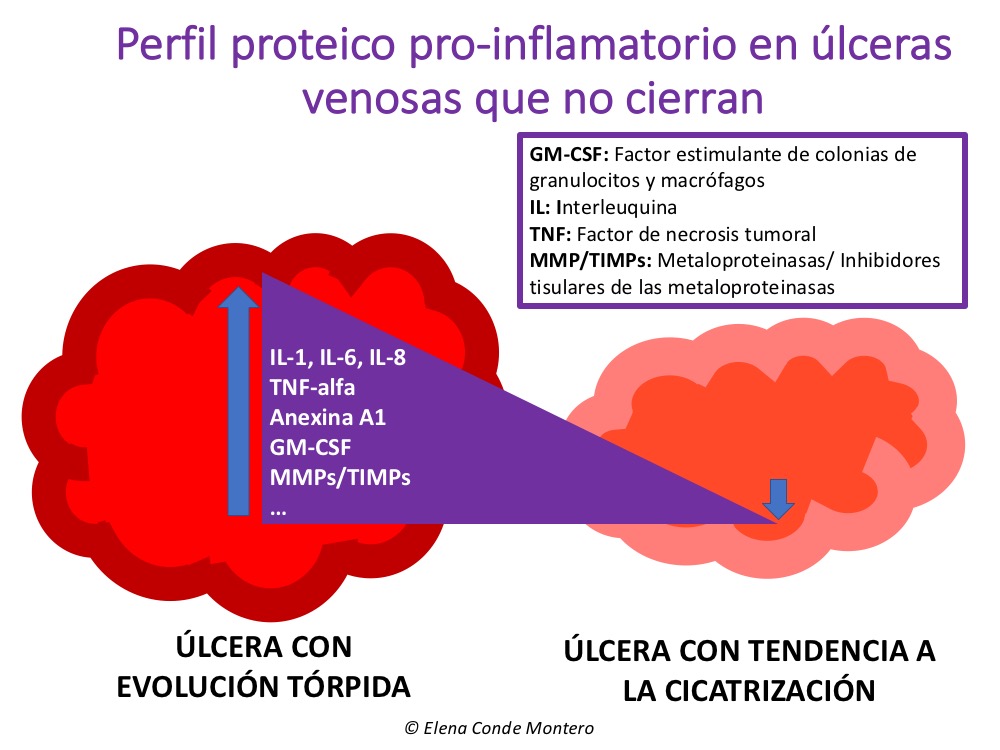
Sabemos que el proteoma es proinflamatorio y proteolítico. Es decir, si estudiamos los tipos de proteínas presentes en el exudado y el lecho de estas heridas, nos encontraremos gran cantidad de proteínas que regulan la actividad de otras células para producir inflamación (citoquinas proinflamatorias) y enzimas que degradan proteínas tisulares (metaloproteinasas). Estas proteínas son producidas predominantemente por los macrófagos, pero también por otras células como neutrófilos, linfocitos, células endoteliales o queratinocitos. Como ya comentamos en entradas previas (Las metaloproteinasas en las heridas crónicas: el problema de una actividad destructiva descontrolada, Herida crónica = inflamación crónica), este tipo de “proteínas destructivas” es fundamental, de manera limitada en el tiempo, en la fase inflamatoria de cualquier herida. El problema es cuando se mantienen en niveles elevados de manera crónica y no dan paso a las “proteínas procicatrización”.
Hay un creciente interés en encontrar predictores moleculares de la evolución de la úlcera venosa. De hecho, hay intentos continuados de realizar una lista de proteínas que se correlacionen con la evolución de la herida. Esto es complicado teniendo en cuenta el dinamismo de la producción proteica, las interacciones entre proteínas, las bajas concentraciones de algunas de ellas, las limitaciones de los diferentes métodos de medición…1,2 En esta línea, se acaba de publicar un estudio que compara las proteínas del exudado de úlceras venosas con y sin tendencia a la cicatrización.3 A pesar de sus limitaciones, sus hallazgos son interesantes. Se incluyen 42 úlceras y, además de registrar la evolución en el área de las lesiones, se toman muestras de exudado semanalmente, durante 3 meses, para medir una amplia batería de proteínas (citoquinas, proteasas y factores de crecimiento). Entre los resultados del trabajo destaca el hallazgo, en las úlceras con mala evolución, de una mayor concentración de metaloproteinasa-13 (MMP-13) y factor estimulante de colonias de granulocitos y macrófagos(GM-CSF), ambos asociados con los macrófagos “destructores” tipo 1, de los que ya hablamos en el post “Herida crónica= inflamación crónica”.
¿Y cuándo se empieza a desarrollar este ambiente proinflamatorio en una pierna con enfermedad venosa crónica? ¿En qué estadio de la clasificación CEAP tiene su origen todo esto? (Ver post “Clasificación CEAP de los trastornos venosos crónicos: hablemos todos el mismo idioma”). Pues en los primeros estadios… La hipertensión venosa, aunque sea incipiente, empieza a dañar el endotelio de las venas, rompiendo las uniones celulares y aumentando la permeabilidad de la pared. Además, activa receptores de la superficie del endotelio (como selectinas o moléculas de adhesión celular) que dificultan el desplazamiento de los leucocitos (linfocitos neutrófilos, macrófagos) por los vasos, hacen que se adhieran a la pared y facilitan su salida a los tejidos circundantes… Todo esto con la consiguiente liberación de proteínas proinflamatorias y destrucción de la pared venosa y del tejido adyacente.


¿Cuánto pesa la carga genética para desarrollar enfermedad venosa y cuánto la carga epigenética, es decir, los factores ambientales? Un campo apasionante para seguir investigando, en el que la proteómica nos puede dar muchas claves.
¿Cómo podemos realizar modificaciones proteómicas en las úlceras venosas?
Por lógica, atacando a la causa de estas modificaciones, que es la hipertensión venosa. ¡Toda recomendación que implique promover el retorno venoso y vencer la gravedad cuanto antes será recomendable!
De hecho, como acabamos de ver, la hipertensión venosa es la responsable del ambiente proinflamatorio que caracteriza a estas heridas. Por tanto, todas las medidas que adoptemos para controlar la hipertensión venosa formarán parte de la “estrategia antiinflamatoria” contra la úlcera venosa.
Si vamos más allá de la lógica y nos centramos en las medidas que, a nivel proteómico, han mostrado interés, hemos de decir que todavía hay mucho que estudiar. Sin embargo, es muy interesante entender la acción a este nivel de la terapia compresiva, desde estadios iniciales de la enfermedad venosa. En el estudio presentado por el Dr. Rodrigo Rial, Modulación Proteómica y Epigenética tras terapia compresiva en la EVC (MoPrETec), se compara el proteoma en las varices extirpadas quirúrgicamente tras 12 semanas de terapia compresiva (media clase II) o 12 semanas sin compresión. Entre sus resultados destaca la disminución, en el grupo con media de compresión, de la p-selectina, proteína relacionada con la adherencia y migración de los leucocitos por el endotelio (en otras palabras, menos inflamación).
Con respecto al proteoma de la úlcera venosa, se ha publicado un estudio que compara el perfil de citoquinas en biopsias de tejido de heridas (30 lesiones incluidas) antes y después de 4 semanas de terapia compresiva (vendaje múltiple cambiado semanalmente), que halla disminución de citoquinas proinflamatorias y aumento de citoquinas antiinflamatorias.4
Por ello, ante la pregunta “¿cuándo empezar con terapia compresiva y medidas antigravedad?” La respuesta siempre será “Cuanto antes, mejor”. Y la respuesta a “¿cuándo acabar?” será “Nunca”. La enfermedad venosa es progresiva ¡Hay que frenar su poder destructivo lo antes posible y mantenerla controlada para evitar recidivas!
El estudio de la proteómica tendrá especial interés en el subgrupo de pacientes con úlcera venosa que, a pesar de una adecuada terapia compresiva y correcto manejo local, no mejoran (Os recomiendo este documento sobre heridas “súper crónicas”). No podemos olvidar que las proteínas que encontramos en la herida venosa serán la expresión de todos los factores que están influyendo en ese paciente (biopelículas, daño tisular, edad, genética, comorbilidades, factores psico-sociales), no sólo la hipertensión venosa.
Es esencial identificar tipos, niveles y actividad de biomarcadores cuya medición sea simple y coste-efectiva para que se pueda aplicar en la práctica clínica. Servirían, por un lado, como herramientas de evaluación evolutiva y, por otro, como dianas terapéuticas para intentar diseñar “tratamientos a medida”.
No es trabajo fácil, ya que el microambiente de la úlcera venosa es muy dinámico, en el que se están generando y destruyendo constantemente proteínas, fruto de una interacción continua entre células del organismo y bacterias. Además de hacer la “foto de las proteínas” de la herida, también sería interesante estudiar los metabolitos que se están generando por los procesos celulares, incluidos bacterianos, que tienen lugar en ese lecho… Estaríamos hablando ya de metabolómica y degradómica… ¡Es la era de las ciencias ómicas en el mundo de las heridas?!Por ahora hay muchas más preguntas que respuestas…
Para acabar, me gustaría agradecer de corazón la invitación para participar en el IV Congreso de la Sociedad Gallega de Heridas. Ha sido un enorme placer hablar de lo que más me gusta en un congreso tan bien organizado. Yo soy coruñesa y siempre es una gran alegría poder disfrutar de Galicia. El bonito recuerdo de los organizadores del congreso ya está colocado en nuestra consulta de heridas en el Centro de Especialidades Vicente Soldevilla.

Referencias:
- Broszczak DA, Sydes ER, Wallace D, Parker TJ. Molecular Aspects of Wound Healing and the Rise of Venous Leg Ulceration: Omics Approaches to Enhance Knowledge and Aid Diagnostic Discovery. Clin Biochem Rev. 2017;38(1):35–55.
- Mannello F, Ligi D, Canale M, Raffetto JD. Omics profiles in chronic venous ulcer wound fluid: innovative applications for translational medicine. Expert Rev Mol Diagn. 2014 Jul;14(6):737-62.
- Stacey MC, Phillips SA, Farrokhyar F, Swaine JM. Evaluation of wound fluid biomarkers to determine healing in adults with venous leg ulcers: A prospective study. Wound Repair Regen. 2019 Sep;27(5):509-518.
- Beidler SK, Douillet CD, Berndt DF, et al. Inflammatory cytokine levels in chronic venous insufficiency ulcer tissue before and after compression therapy. J Vasc Surg 2009;49(4):1013-20.







Coincido con la Dra. Conde en la excelencia que demostró el DR. Rial en su ponencia del congreso de la SGH en Vigo,… Siempre es un placer tener la oportunidad de poder aprender de maestro como ustedes.
Enhorabuena por su trabajo en la divulgación del conocimiento.
Muchas gracias, Estrella